Синдром патау: что это такое, симптомы, способы диагностики и лечения, прогноз
Содержание:
Синдром Патау у детей: лечение
Вылечить синдром Патау нельзя. Заболевание неизлечимое, так как наблюдаются нарушения в развитии и строении внутренних органов.
Распространенные операции при синдроме Патау:
- Пластика лица. Так как при этом недуге часто имеются расщелины на губах, проводится их пластика.
- Операции на внутренних органах. Обычно оперируют почки, мочеточники и сердце. Врачи пытаются облегчить уход за ребенком.
- У девочек удаляется дополнительная матка. Также проводится удаление кист.
- Вообще все лечение направлено на устранение симптомов недуга и укрепление иммунитета. Облегчить состояние ребенка необходимо чтобы избежать воспаления и без того нездоровых органов. Касательно умственного развития, то такие дети недоразвитые и не смогут жить полноценной жизнью.
Синдром Патау – серьезное генетическое нарушение, которое делает ребенка не самостоятельным. Именно поэтому врачи рекомендуют прерывание беременности на сроке до 22 недель.
Подготовка к амниоцентезу
Для повышения эффективности исследования и уменьшения рисков возможных осложнений пациентка должна осуществить следующие подготовительные мероприятия:
- Пройти консультацию у врача, на которой он подробно расскажет о прохождении процедуры, ее возможных осложнениях, противопоказаниях и т. д.
- Сдать анализы и пройти УЗИ, позволяющие выявить скрытые инфекционные или воспалительные заболевания, наличие новообразований, объем околоплодных вод, подтвердить или опровергнуть многоплодную беременность. Также с их помощью определяется срок беременности, состояние и жизнеспособность плода.
- Примерно за 4-5 дней до проведения амниоцентеза пациентка должна исключить прием ацетилсалициловой кислоты или аналогичных ей препаратов, за 12-24 часа – прекратить употребление препаратов, снижающих свертываемость крови для уменьшения риска кровотечений.
Эти мероприятия необходимо выполнить для того, чтобы повысить безопасность амниоцентеза, снизить риск появления осложнений у самой женщины и ее ребенка, увеличить эффективность диагностики.
Причины развития заболевания
Как уже упоминалось, синдром Патау характеризуется трисомией тринадцатой пары хромосом. При этом в большинстве случаев (согласно статистике, в 80 %) имеет место нерасхождение тринадцатой хромосомы именно в процессе мейоза. Чаще всего ребенок получает полную пару хромосом от матери. Иногда имеет место робертсоновская транслокация, при которой уже зародыш получает дополнительную копию генов.
Доказано, что генетический сбой может произойти во время формирования гаметы или позднее — при образовании зиготы.
На сегодняшний день причины появления мутации не установлены — считается, что она возникает абсолютно случайно. Также неизвестна роль инфекций, вредных привычек, соматических заболеваний матери в процессе развития данной патологии у плода.
Описание
Резус-фактор (Rh) — это антиген (белок), который находится на поверхности эритроцитов, причём наиболее иммуногенным является антиген D (RhD), присутствие которого и определяет положительный резус-фактор (Rh+). Исследование выполняется с 9 полных недель беременности, т. е. с 10 недели.Для проведения исследования необходимо предоставить копию УЗИ.
Если резус-отрицательная (Rh-) женщина беременна резус-положительным (Rh+) плодом, её иммунная система начинает вырабатывать анти-D-антитела, вызывающие разрушение эритроцитов плода. Как правило, анти-D-антитела отсутствуют при первой беременности Rh+ плодом, протекающей без осложнений, однако сенсибилизация матери возникает в процессе родов. При каждой последующей беременности или при повреждении плаценты увеличивается риск развития гемолитической болезни плода. 98% случаев гемолитической болезни новорождённых связаны именно с D-резус-антигеном. При раннем проявлении резус-конфликт может стать причиной нарушения развития плода, преждевременных родов или выкидышей.Ген RHD
Делеция гена RHD в обеих гомологичных хромосомах обуславливает отрицательный резус-фактор. Наличие гена в гомозиготном или гетерозиготном состоянии определяет положительный резус-фактор у обследуемого. В случае если резус-положительные отцы являются гетерозиготными по резус-фактору, то у резус-отрицательных матерей даже при наличии отягощённого анамнеза плод в 50% случаев будет резус-отрицательным. Таким образом, для женщин с резус-конфликтной беременностью появилась возможность проведения пренатальной диагностики с целью определения резус-фактора на ДНК плода, выделенной из ворсин хориона (10–15 недель беременности) или из амниотической жидкости при проведении амниоцентеза (24 неделя беременности).
Если результаты молекулярно-генетического анализа показывают, что плод является резус-отрицательным, то отпадает необходимость в проведении последующих инвазивных процедур, и такие пациентки исключаются из дальнейшего обследования по тяжести развития гемолитической болезни плода. Кроме того, определение гетерозиготного генотипа по резус-фактору (RHD+/RHD-) у отца даёт основание для проведения преимплантационной диагностики при наличии отягощённого акушерского анамнеза (гибель детей от гемолитической болезни) и резус-сенсибилизации у матери. В результате при ЭКО будущей матери будут перенесены только резус-отрицательные эмбрионы.
Так как антирезусную профилактику иммуноглобулином человека рекомендовано проводить на 28 неделе первой и последующих беременностей, то определение резус-фактора плода на ранних сроках является необходимым. Определение Rh- плода в 1–2 триместре беременности позволит сократить расходы на регулярное определение титра анти-D-антител и антирезусную профилактику.Показания
Беременным (Rh-)-женщинам с 12 по 27 неделю беременности, если (Rh+)-отец является гетерозиготным носителем гена RhD (Генотипирование системы RhD).Подготовка
Специальная подготовка не требуется. Рекомендуется взятие крови не ранее чем через 4 часа после последнего приема пищи.Интерпретация результатов
При отрицательном результате теста, статус плода считается с высокой вероятностью резус-отрицательным, однако рекомендуется повторять тест на более поздних сроках беременности (но не позднее 27-ой недели) для подтверждения.
Положительный результат теста считается показанием к введению антирезусного иммуноглобулина, однако вопрос о его введении должен решаться только акушером-гинекологом на основании и других методов диагностики резус-конфликта.
При отсутствии антител к Rh-фактору по результатам ИФА и положительном молекулярно-генетическом тесте, рекомендуется введение антирезусного иммуноглобулина в период от 28 недель беременности (для профилактики ГБН) и не позднее 72 часов после родов (для профилактики Rh-конфликта при следующей беременности).
Преимущества теста НИПТ:
Это позволяет заблаговременно спланировать место появления ребенка на свет и быть готовыми своевременно оказать малышу необходимую медицинскую помощь в требуемом объеме. Проводить такие роды и вести ранний неонатальный период таких «особенных» малышей призваны Перинатальные центры, оснащенные всем необходимым оборудованием и имеющие профильных опытных специалистов.
Своевременная информация о состоянии здоровья плода бесценна, она дает возможность и время родителям на то, чтобы осознать проблему, провести необходимые дообследования и консультации и принять наиболее правильное решение, подготовиться к родам, спланировать последующие после родов мероприятия.
Симптомы
Симптомы данного синдрома при беременности:
Для этого синдрома у новорожденных характерны следующие симптомы:
Очень часто при данном синдроме у новорожденных наблюдаются различные пороки развития сердца: транспозиции сосудов, дефекты в развитии межпредсердной и межжелудочковой перегородок и др.
Хотя новорожденные с таким синдромом, в большинстве случаев, умирают в течение года, в развитых странах продолжительность жизни может достигать пяти, а иногда и десяти лет. Но, такие дети страдают глубокой идиотией.
Люди с такими нарушениями склонны к развитию различных видов острых миелоидных лейкозов.
В чем преимущества пренатального генетического теста?
Если женщина выполняет неинвазивный генетический анализ крови, мы, скорее всего, узнаем, есть ли у ребенка какие-либо генетические дефекты или нет. Раннее, до родов, выявление генетического дефекта позволяет врачам спланировать надлежащий уход за такой пациенткой во время беременности и родов, а также провести соответствующее лечение или профилактику (если возможно). Родители, в свою очередь, получают возможность подготовиться к ребенку с особыми потребностями.
Однако следует подчеркнуть, что генетические тесты крови не дают стопроцентной уверенности – для ее получения необходимо провести инвазивный тест, например, амниоцентез или забор проб ворсин хориона.
Что оценивается при УЗИ в 1 триместре
1. Копчико-теменной размер (КТР) плода
Этот показатель точно определяет срок гестации (беременности), особенно в случае, если женщина не помнит 1-й день последней менструации, либо если менструальный цикл у нее не регулярный. В заключении срок беременности выставляется по КТР плода, а не по дате последней менструации.
Правильное измерение КТР плода
2. Маркеры хромосомной патологии:
— толщина воротникового пространства (ТВП) – является основным признаком хромосомной патологии у плода. Патологической величиной считается увеличение ТВП больше 95-й процентили для каждого срока гестации. Каждое увеличение ТВП повышает риск существования хромосомной аномалии у плода.
ТВП в норме ТВР при патологии
Важно понимать, что увеличение ТВП — это признак (маркер), но не точная диагностика хромосомных аномалий у плода. Определить наличие синдрома Дауна и других заболеваний у будущего ребенка позволяет только инвазивная диагностика с последующим генетическим анализом.. — носовая кость
У плодов с синдромом Дауна носовая кость может отсутствовать, либо быть уменьшенной (гипоплазированной). Очень редко такое может встречаться и у совершенно здоровых детей. Точный диагноз устанавливается только при помощи генетического анализа.
— носовая кость. У плодов с синдромом Дауна носовая кость может отсутствовать, либо быть уменьшенной (гипоплазированной). Очень редко такое может встречаться и у совершенно здоровых детей. Точный диагноз устанавливается только при помощи генетического анализа.
Нормальная носовая кость Отсутствие носовой кости
— кровоток в венозном протоке – это маленький сосуд в печени плода. При обратном (ретроградном) токе крови в данном сосуде можно предположить, что у плода хромосомный синдром, либо врожденный порок сердца.
Нормальный кровоток в венозном протоке
Но важно правильно получить этот кровоток и дать ему оценку. Для этого требуются определенные навыки и квалификация врача, которые подтверждаются ежегодной сертификацией FMF.. — кровоток через трикуспидальный клапан в сердце плода
Здесь ретроградный (обратный) кровоток тоже указывает на хромосомную патологию, либо может проявляться при врожденных пороках сердца.
— кровоток через трикуспидальный клапан в сердце плода. Здесь ретроградный (обратный) кровоток тоже указывает на хромосомную патологию, либо может проявляться при врожденных пороках сердца.
Ручка плода Мозг плода в виде “бабочки” в норме
Профилактика
На данный момент не существует профилактики по предупреждению развития данного синдрома.
Синдром Патау: виды, причины, симптомы, диагностика, лечение и профилактика
Цитогенетическая форма – развивается в результате наличия копии лишней 13 хромосомы при нерасхождении хромосом или робертсоновской транслокации.
Простая форма – нарушения происходят на ранних этапах развития плода. Каждая клетка при такой форме несет в себе лишнюю хромосому.
Мозаичная форма – нарушения образуются на более поздних этапах формирования плода, что приводит к развитию отдельных областей с здоровыми клетками и областей, в которых присутствуют патологичные клетки. Характерно медленное развитие патологических изменений в организме. Иногда патологии при данной форме заболевания могут быть очень слабо выражены.
- в процессе деления половой клетки возможно нерасхождение хромосом;
- робертсоновская транслокация, при которой зародыш получает дополнительно копию генов;
- различные аномалии, которые образуются на уровне содержания генетической информации в клетке;
- различные мутационные изменения;
- мутации оплодотворенной яйцеклетки;
- мутации клеток плода.
- плохая экологическая ситуация района проживания;
- дети, которые родились от браков между близкими родственниками;
- наличие наследственных заболеваний во всех предыдущих поколениях родителей;
- пожилой возраст матери (данная болезнь диагностируется у детей, которые были рождены женщинами после 45 лет).
- время беременности сокращается (составляет 38,5 недель);
- многоводие;
- выкидыш;
- мертворождение.
- недоразвитость (истинная пренатальная гипоплазия);
- различные тяжелые врожденные пороки;
- низкая масса тела при рождении;
- нарушение строения черепа;
- умеренная микроцефалия;
- флексорное положение кистей;
- различные нарушения строения рук (например, полидактилия);
- различные нарушение развития ЦНС;
- низкий и скошенный лоб;
- расстояние между глазными щелями уменьшено;
- суженные глазные щели;
- колобома;
- помутнение роговицы;
- микрофтальмия;
- основание носа широкое;
- ушные раковины деформированные;
- запавшая переносица;
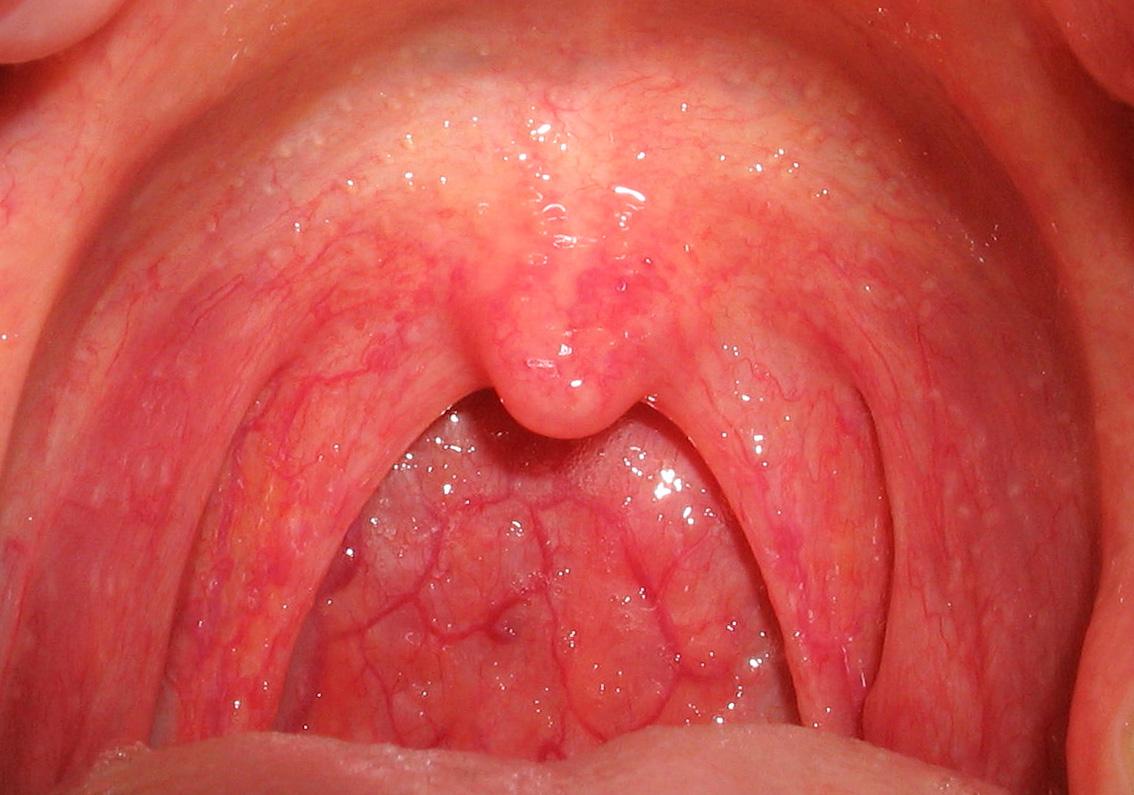
- расщелина верхней нёба и губы;
- короткая шея;
- гипопитуитаризм;
- изменения поджелудочной железы (фиброкистозные);
- гетеротопия поджелудочной железы;
- возможно наличие добавочные селезенки;
- почки увеличены;
- пупочная эмбриональная грыжа;
- кисты в корковом слое почек;
- аномалии развития половых органов.
- ультразвуковое исследование;
- генетическое исследование наследственного материала на наличие лишней 13 хромосомы;
- биопсия ворсинок хориона (БВХ);
- амниоцентез;
- кордоцентез.
3.Симптомы и диагностика
Осевым, синдромообразующим симптомом болезни Лане выступает пятнистая эритема на ладонях и подошвах, т.е. участки интенсивного красного цвета с малиновым оттенком. В действительности такие очаги образованы множеством мелких близкорасположенных красно-малиновых точек. К характерным и ключевым для дифференциальной диагностики особенностям заболевания относится резкая, без плавного перехода, граница между пораженными и здоровыми участками кожи, отсутствие мацерации (мокнутия) и потливости, а также отсутствие аналогичных эритематозных участков на ступнях, тыльной части ладоней и каких бы то ни было иных участках тела.
Эритроз Лане никогда не сопровождается болевым синдромом либо какими-то дискомфортными ощущениями. В атипичных случаях иногда отмечается утолщение рогового, наружного слоя эпидермиса, тенденция к отшелушиванию или потливость, волнообразное течение (эритематозные поверхности то немного светлеют, то вновь обретают интенсивный оттенок).
Указанные выше особенности в сочетании с результатами внешнего осмотра служат достаточным основанием для установления диагноза.
Типы наследственных заболеваний
Наследственные заболевания делятся на три типа: моногенные, полигенные (или многофакторные) и хромосомные. В основе моногенных заболеваний лежит мутация одного гена, которая локализована в одной хромосоме и провоцирует обменные процессы в организме.
Моногенные и полигенные генетические болезни
К моногенным наследственным заболеваниям относятся: синдром Марфана, хорея Гентингтона, муковисцидоз, фенилкетонурия, миопатия Дюшена, гемофилия и др. При полигенных (многофакторных) болезнях с наследственной предрасположенностью соотношение больных не соответствует теории расщепления, которую придумал основоположник генетики Г.И. Мендель. Для патологического проявления мутантного гена обязательно действие специфического внешнего фактора, например лекарственных препаратов (тератогенное действие), химических веществ или биологических агентов. Без воздействия специфического фактора даже при наличии в генотипе мутантного гена заболевание не развивается. Полигенные болезни обусловлены взаимодействием нескольких генов с факторами окружающей среды. К полигенным наследственным болезням относятся гипертоническая болезнь, атеросклероз, язвенная болезнь желудка и двенадцатиперстной кишки, сахарный диабет обоих типов, аллергические заболевания, гепатит, ревматоидный артрит, лейкоз, ишемическая болезнь сердца, онкологические заболевания, психические расстройства и др.
Хромосомные болезни
К хромосомным относят болезни, связанные с геномными мутациями или структурными изменениями отдельных хромосом. Возникают они в результате мутаций в половых клетках одного из родителей. Из поколения в поколение передаются не более 3-5% из них. Хромосомные нарушения приводят к 50% спонтанных абортов, и 7% всех мертворождений. Хромосомные болезни возникают как из-за изменения количества и структуры хромосом, так и нерасхождением хромосом на ранней стадии дробления зиготы, которые приводят к развитию мозаицизма, а также из-за ломкости Х-хромосомы.
Из числа количественных нарушений хромосом общеизвестны такие болезни, как болезнь Дауна (трисомия по 21-й хромосоме), синдром Эдвардса (трисомия по 18-й хромосоме), синдром Патау (трисомия по 13-й хромосоме), синдром Шерешевского-Тернера (отсутствие одной Х хромосомы у женщин), синдром Клайнфельтера (лишняя Х-хромосома у мужчин), синдром дисомии по У-хромосоме у мужчин.
К внутрихромосомным мутациям относятся болезни: синдром-Прадера-Вилли (отсутствие 7-ми генов из 15-й хромосомы), синдром Ангельмана (критичность региона 15-й хромосомы материнского происхождения). Структурные нарушения хромосом приводят к таким болезням, как синдром «Кошачьего крика» (утрата короткого плеча 5-й хромосомы), а ломкость Х-хромосомы к одноименной болезни (синдром Мартина-Белла). Примерно у 30-40% больных с синдромом ломкой Х-хромосомы клиническая картина имеет выраженный шизофреноподобный характер, в первую очередь это аутистические признаки и двигательные расстройства кататоноподобного характера.
Отдельно хочется сказать о дисомии по У-хромосоме, поскольку это заболевание, вызванное добавочной У-хромосомой у мужчин, может привести к опасным последствиям. Признаками кариотипа 47 ХУУ являются высокий рост (186-200 см), акромегалия, непропорциональное увеличение дистальных отделов конечностей, физическая сила, интеллект не ниже среднего. Лишняя У-хромосома определяет эмоционально-волевые нарушения, приводит к агрессии, многие обладают способностью давить на психику взглядом. Если произойдет сбой, то возможны однотипные, серийные преступления. За всю историю криминалистики среди серийных убийц с помощью скрининга был выявлен лишь один человек с лишней У-хромосомой. Если обследование подтверждает у убийцы наличие лишней У-хромосомы, то его отправляют не за решетку, а в клинику. Из мирового кинематографа известен такой представитель кариотипа 47 ХУУ, как Доктор Ганнибал Лектер из «Молчания ягнят».
Как проводится тест Prenetix в клинике «Линия жизни»?
Какой-то подготовки тестирование не требует. Единственная рекомендация – анализ сдается натощак, накануне следует избегать жирной пищи. Чтобы сдать анализ, беременная женщина приходит к нам в клинику. Специалист берет у неё кровь из вены, после этого будущая мама отправляется домой, а образец крови передается генетикам.
Специалисты выделяют из материнской крови макромолекулу ДНК плода и исследуют её по технологии NGS (секвенирование нового поколения). Этот передовой метод с точностью более 99% выявляет риски наличия и развития хромосомных патологий. Дополнительно, по желанию родителей, специалисты могут определить пол малыша. Здесь точность составляет уже 100%.
По результатам анализа генетик готовит заключение, которое выдается на руки родителям (информация конфиденциальна, больше никто не имеет к ней доступа). Результаты теста готовы через 10 дней после сдачи крови.
Плюсы неинвазивной пренатальной диагностики в центре «Линия жизни», Москва
- Безопасность для ребёнка. Неинвазивное исследование не предполагает никакого воздействия на плод. В отличие от инвазивных методик «Пренетикс» не затрагивает органы и ткани малыша.
- Безболезненность для будущей мамы. В «Линии жизни» кровь на анализ берут опытные медицинские сестры. Для точного тестирования достаточно 20 миллилитров венозной крови.
- Ранний срок диагностики. Тест можно проводить, начиная с 10-й недели беременности.
- Точность. Практически всегда Prenetix ставит точку в постановке диагноза. Вероятность ошибок не превышает 0,1%.
Почему цена теста Prenetix полностью оправдана?
По данным ВОЗ, каждый год от врожденных пороков развития погибает 3,3 миллиона малышей до 5 лет. Выживает при врожденных пороках примерно столько же, но живут такие дети с инвалидностью, часто очень тяжёлой. Неинвазивный пренатальный ДНК тест позволяет заранее выявить хромосомные аномалии.
- Синдром Дауна 1:700
- Синдром Шерешевского-Тернера 1:1500
- Синдром Клайнфельтера 1:700
- Синдром Эдвардса 1:6000
- Синдром Патау 1:7000
Во-первых, важно снять тревожность у будущей мамы. Если беременность долгожданная, она может сопровождаться многочисленными переживаниями за здоровье малыша, а маме важно беречь себя от стресса
Необходимо пройти тест Prenetix и успокоиться.
Во-вторых, при многих хромосомных отклонениях возможно достаточно высокое качество жизни
И тут важно, чтобы семья была готова к диагнозу, ведь малыш будет нуждаться в особой поддержке и специализированной медицинской помощи с самого рождения. Prenetix позволяет выполнить это условие
Если учесть все преимущества теста, его достоверность и важность для родителей, вывод очевиден – цена диагностики полностью оправдана
Применение амниоцентеза
Амниоцентез при беременности используется прежде всего как диагностическая процедура для выявления некоторых генетических нарушений у плода — например:
- Синдрома Дауна, характеризующегося отклонениями в умственном развитии, пороками внутренних органов и аномальными особенностями внешности;
- Синдрома Патау, для которого характерны внешние аномалии, нарушения развития ЦНС и мозга, несовместимые с жизнью (новорожденный умирает спустя несколько дней);
- Синдрома Эдвардса, сопровождающегося нарушениями в строении внутренних органов (чаще всего сердца), задержкой умственного развития, ранней смертностью (средняя продолжительность жизни таких детей — несколько месяцев);
- Синдрома Тернера, проявляющегося исключительно у девочек в виде пороков развития внутренних органов, бесплодием, низкорослостью (хотя люди с такой патологией не имеют отклонений в интеллектуальном развитии и могут вести полноценную жизнь);
- Синдрома Клайнфельтера, характерного только для мужчин и сопровождающегося удлинением конечностей, высоким расположением талии, гинекоматией, замедленным половым созреванием, атрофией яичек, бесплодием.
Помимо выявления генетических аномалий у плода, амниоцентез при беременности применяется для контроля общего развития органов и систем ребенка у женщин, входящих в группы риска.
Показаниями к амниоцентезу являются:
- Наличие у беременной женщины или ее родственников генетических аномалий;
- Возраст женщины, превышающий 35-летнюю отметку (после нее повышается риск образования в яичниках лишней 21 хромосомной пары);
- Результаты ультразвукового обследования — например, выявление увеличенного просвета между шейной костью и кожей плода, характерного для синдрома Дауна;
- Результаты биохимического скрининга — превышение нормального уровня ХГЧ или аномально низкая концентрация РАРР-А (специфического белка, содержащегося в плазме крови).
Еще одной областью использования этой методики является искусственное прерывание беременности. В этом случае с помощью пункционной иглы в амниотическую жидкость вносятся растворы препаратов, убивающих плод и способствующих его отторжению и изгнанию из матки.
Лечение
Вылечить синдром Патау невозможно. Патология приводит к возникновению нарушений в развитии и строении внутренних органов. Медики могут попытаться облегчить состояние ребенка. Для этого проводится оперативное вмешательство. Чаще всего при синдроме Патау выполняется:
- Пластика лица. У многих пациентов при этом недуге наблюдаются расщелины на губах. Врачи устраняют этот недостаток.
- Удаление дополнительной матки. Аналогичное действие выполняется в отношении других подобных патологий, если они имеют место быть.
- Проводятся операции на внутренних органах. Обычно лечение осуществляется в отношении почек, мочеточников и сердца. Это позволяет облегчить уход за ребёнком.
Дополнительно проводится симптоматическое лечение. Врачи устраняют сопутствующие симптомы и укрепляют иммунитет ребенка. Действия необходимо выполнять для того, чтобы избежать воспаления органов. Дети с синдромом Патау всегда недоразвитые. Это касается физического и умственного развития. Полноценной жизнью жить такие пациенты вряд ли могут. Ребёнок не будет самостоятельным. Именно поэтому врачи рекомендуют прервать беременность на сроке до 22 недель.
Виды пренатального тестирования
Пренатальное тестирование делится на две группы:
- неинвазивное;
- инвазивное.
В первую входят тесты, которые чаще всего проводят при каждой беременности, независимо от факторов риска пороков развития. Это:
- УЗИ – пренатальное УЗИ;
- биохимические исследования крови матери.
Существуют также неинвазивные скрининговые тесты (тест PAPP-A), которые могут выявить синдром Дауна, а также синдромы Эдвардса и Патау.
В соответствующий период беременности – от 11 до 13 недель и 6 дней беременности – также проводится ультразвуковое исследование для оценки дефектов и анализ крови для измерения уровня белка PAPP-A и свободного бета-ХГЧ.
НАШИ ПАРТНЕРЫ
Лечение заячьей губы
Устранение такого дефекта, как заячья губа, проводится с помощью пластической хирургии.
Выделяют следующие типы оперативного хирургического вмешательства, применяемые для лечения заячьей губы:
- хейлопластика;
- ринохейлопластика;
- ринохейлогнатопластика.
Если доношенный новорожденный не имеет иных пороков развития, а также противопоказаний к операции, возможно проведение реконструктивной пластической операции уже в течение первого месяца жизни, но обычно детей, страдающих заячьей губой, оперируют в возрасте от 3 до 6 месяцев.
Хейлопластика
Хейлопластика
Современная хейлопластика располагает разнообразными методиками, которые направлены на устранение эстетической и функциональной неполноценности пациента с заячьей губой.
Хейлопластика – это пластическая операция по коррекцию верхней губы. Подобное вмешательство требует предварительного обширного медицинского обследования пациента.
В процессе хейлопластики хирург выполняет сопоставление фрагментов тканей и их соединение. Для максимальной защиты швов в носовую полость необходимо на некоторое время ввести марлевый тампон, который затем извлекается. На его место устанавливается специальная трубка сроком до 90 суток после окончания вмешательства.
Швы после операции снимаются через 10 суток с момента проведения операции по устранению заячьей губы. Иногда после хейлопластики требуется дополнительно медицинское сопровождение для полного удаления любых остаточных явлений данного нарушения.
Ринохейлопластика
Ринохейлопластика – пластическая операция, подразумевающая большую сложность, чем хейлопластика. Подобное вмешательство представляет собой одновременные лечебные хирургические манипуляции, которые направлены не только на устранение заячьей губы, но и на коррекцию носовых хрящей и мышечной части ротовой полости.
Ринохейлогнатопластика
Ринохейлогнатопластика – это особая костная пластическая операция незаращения альвеолярного отростка, являющаяся наиболее сложным вмешательством среди трех возможных вариантов устранения заячьей губы. Она применяется в таких случаях, когда нарушения скелета лица отличаются высокой степенью тяжести.
Операция помогает устранить недоразвитие и деформацию передней части верхней челюсти, она способна улучшить форму верхней губы и уменьшить дефект носовых хрящей, связанный с ней, а также снижает до минимума вероятность развития отклонений челюстно-зубного развития.
Помимо прочего, ринохейлогнатопластика отвечает за формирование мышечного каркаса полости рта в норме. Проведение подобной операции является типичной хирургической практикой для детей, страдающих от расщелины неба или губы.
Эффективность лечения
Заячья губа после операции обычно устраняется полностью в 85-90% случаев. Это гарантирует в будущем нормальную адаптацию растущего человека в социальной среде. Результаты проведенной операции (как функциональные, так и эстетические) оцениваются спустя 12 месяцев со дня ее проведения.
Заячья губа после операции обычно устраняется полностью в 85-90% случаев. Это гарантирует в будущем нормальную адаптацию растущего человека в социальной среде. Результаты проведенной операции (как функциональные, так и эстетические) оцениваются спустя 12 месяцев со дня ее проведения.
Профилактика нарушения
Для профилактики появления патологии будущей маме необходимо:
-
отказаться от вредных привычек;
-
обследоваться на наличие ИППП;
-
избегать стрессов;
-
если в семье есть любое генетическое заболевание, необходимо проконсультироваться с врачом-генетиком.
Отопластика – пластическая операция, занимающая одну из лидирующих позиций на рынке спроса услуг пластической хирургии. Она проводится по разным показаниям и …
Читать далее >>
Пренатальная диагностика
1) Инвазивные исследования (амниоцентез, биопсия хориона) в основном назначают тем женщинам, у которых наблюдается повышенный риск того, что родится малыша с синдромом Патау, например, пациенткам, чей возраст превышает 35 лет или с плохими результатами неинвазивных тестов: УЗИ и анализов. Инвазивные методы диагностики являются высокоточными, однако, учитывая риск осложнений, не подходят для массового проведения всем беременным, а проводятся только по особым показаниям.
2) Неинвазивные технологии, так называемые скрининги. Скрининг – комплексное исследование беременных женщин на наличие у плода хромосомных аномалий. Выделено несколько признаков, указывающих на высокий риск наличия заболевания, которые может выявить УЗИ плода (отсутствие носовой кости, увеличенная толщина воротникового пространства, недостаточная длина бедренных и плечевых костей и другие особенности). В комплексе с УЗИ идёт биохимический анализ крови матери на такие гормоны как свободный бета-ХГЧ и PAPP-A. Полученные данные по биохимическим маркерам анализируют в совокупности с результатами ультразвукового исследования, а результат всего скрининга представляет собой расчет риска наличия хромосомной аномалии у плода.
Однако при использовании стандартных тестов на синдром Патау, лишь у 3% женщин, направленных на инвазивную диагностику действительно подтверждается наличие заболевания. В то же время не исключены и ложно-отрицательные результаты, когда скрининг показывает низкий риск, а ребенок рождается с хромосомной патологией.
- точность 99%, что намного точнее классической диагностики (УЗИ и биохимический скрининг)
- совершенно безопасен, в отличие от инвазивных методик — для забора материала на анализ необходимо просто взять кровь из вены беременной женщины.
- на ранних сроках: анализ можно проводить уже на 9-й неделе беременности.
Москва, ул. 3-я Тверская-Ямская 52 тел. +7 495 777 96 32Политика конфиденциальности персональных данных
DIV >
Патологии плода, вызванные алкогольной зависимостью беременной
Самая распространённая патология, вызванная употреблением алкоголя беременной женщиной, — синдром Миллера-Дикера. Мутация происходит в гене 17-й хромосомы. Главная причина аномалии — интоксикация плода альдегидами, передающимися через материнскую кровь.
На УЗИ синдром Миллера-Дикера выражается в многоводии, отставании внутриутробного развития плода и снижении его двигательной активности. На более поздних сроках можно увидеть утолщение коры головного мозга при разглаживании мозговых извилин.
Голова у больных детей меньше положенного размера, лоб выпуклый, плоский затылок, челюсть недоразвита (алкогольная дизморфия). Ушные раковины расположены ниже положенного уровня, пальцы неправильной формы, тазобедренные суставы находятся на зачаточном уровне, стопы укорочены, задний проход сросшийся.
Такие дети обычно умирают в возрасте в 2 лет из-за аспирационной пневмонии. У них глубокая умственная отсталость и отсутствуют даже обычные рефлексы (глотание, моргание).