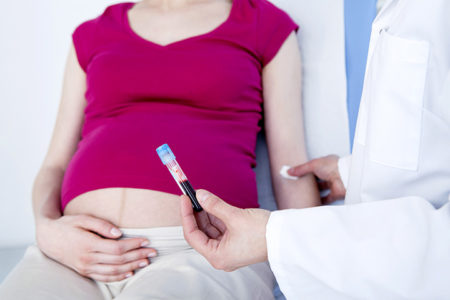
Отрицательный резус при беременности: влияние на вынашивание и роды
Содержание:
Факторы, приводящие к осложнениям беременности
Осложнения во время беременности появляются по самым различным причинам. К наиболее значимым из них относятся:
- Генетические нарушения. Этот фактор может носить как случайный, так и наследственный характер. В первом случае подразумевается патология генов плода, появившаяся в результате их случайной рекомбинации из геномов здоровых родителей в момент оплодотворения. Наследственные генетические нарушения передаются эмбриону от его матери и отца, при этом в семье они могут наблюдаться в течение нескольких поколений. Например, наличие родственников с задержкой умственного развития повышает генетический риск осложнения беременности с патологией плода аналогичного характера.
- Инфекции. Вирусные, бактериальные, грибковые заболевания — частая причина патологий, возникающих во время беременности. Попадая в организм матери, инфекционные возбудители провоцируют иммунный ответ, который может воздействовать и на ребенка. Сами они также оказывают негативное влияние на здоровье плода, причем на всех стадиях его развития — от зачатия до родов. Инфекции могут вызывать различные патологические явления в репродуктивной системе женщины, мешающей ей нормально зачать, выносить и родить здорового малыша.
- Заболевания различной природы. Помимо инфекций, негативно повлиять на протекание беременности могут другие врожденные и приобретенные патологии. Сахарный диабет, высокое артериальное давление (гипертензия), аномалии развития органов репродуктивной системы, заболевания сердца и сосудов, почек, печени, доброкачественные и злокачественные новообразования, психические нарушения часто приводят к выкидышам, физической или психической неполноценности рожденного ребенка.
- Вредные привычки. Употребление алкоголя и наркотических веществ (особенно систематическое), курение одного или обоих родителей — еще один распространенный фактор, вызывающий патологии беременности. Этиловый спирт, психотропные вещества, никотин, а также находящиеся в составе спиртных напитков, сигарет и наркотиков примеси обладают канцерогенным и тератогенным действием. Помимо непосредственного риска выкидыша или замершей беременности, они оказывают долгосрочные эффекты, которые могут проявиться у ребенка в подростковом или взрослом возрасте. Одним из самых частых таких последствий является алкогольный синдром плода, проявляющийся в задержке умственного развития, лицевые дефекты, антисоциальное поведение.
- Прием лекарственных препаратов. Осложнить зачатие, вынашивание и роды могут медикаменты, которые принимает женщина в период вынашивания ребенка. К сожалению, многие лекарства имеют выраженный тератогенный эффект, который необходимо учитывать при их назначении. При выпуске каждого препарата предусмотрены его клинические испытания на выявление побочных воздействий на плод. Проблема в том, что далеко не все производители фармацевтики проводят полноценные тесты на тератогенность. Например, широко известна история со снотворным “Талидомид”, который в середине прошлого века привел к массовым случаям рождения детей с аномалиями развития в США.
- Возрастные изменения. Оптимальный возраст для вынашивания здорового ребенка — 20-35 лет. В этот период репродуктивная система женщины наиболее активна, а сама будущая мама психологически подготовлена к беременности. Более ранний и поздний срок наступления беременности существенно повышает риск выкидыша или рождения ребенка с пороками развития. Так, зачатие после 35 лет увеличивает вероятность появления малыша с синдромом Дауна. Ранняя беременность также несет определенные риски, связанные с незрелостью репродуктивной системы будущей мамы.
- Социальное положение. На течение беременности оказывает влияние условия, в которых живет будущая мама. Низкое социальное положение, тяжелая работа, недоедание повышают физическую и эмоциональную нагрузку на женщину. Малый финансовый доход ограничивает ее доступ к современной медицине, заставляет трудиться в период вынашивания, в том числе заниматься предоставлением сексуальных услуг за деньги. Кроме того, часто матери живут в антисанитарных условиях, где велика вероятность заболеть инфекцией.
Среди прочих факторов, повышающих риск осложнения беременности, можно упомянуть неблагоприятную экологическую обстановку, сильный и/или постоянный эмоциональный стресс, случайно или намеренно нанесенные (в том числе посторонними лицами) травмы, нерациональное питание и т. д. Эти причины могут наблюдаться у конкретной женщины как по-отдельности, так и в комплексе — во втором случае существенно усложняется диагностика патологий.
Методы лечения
Резус конфликтная беременность требует особого внимания со стороны врачей. Если в крови женщины были обнаружены антирезус-антитела или специалисты установили признаки гемолитической болезни у ребенка, проводится неспецифическое лечение. Схема терапии в таком случае:
|
Метод лечения |
Описание |
|
Медикаментозное лечение |
|
|
Физиотерапия |
|
|
Диета |
В рацион обязательно вводят недожаренную печень или печеночные экстракты. |
|
Диатермия околопочечной области |
Это метод физического лечения, при котором указанную область прогревают при помощи токов высокой частоты. Процедура назначается при высоком риске самопроизвольного выкидыша. |
|
Досрочные роды |
Показаны при неэффективности предыдущих методов. Проводятся двумя способами:
|
Существует и специфическое лечение резус-конфликта. В отличие от неспецифических мер, оно имеет несколько иные показания. Такое лечение назначают всем женщинам с отрицательным резусом в следующих случаях:
- после родов, выкидышей, абортов;
- после оперативного лечения внематочной беременности.
Специфическая терапия – это внутримышечное введение антирезусного иммуноглобулина сразу после родов или операции. Инъекция должна быть сделана не позже 48–72 ч. после медицинских манипуляций. В противном случае препарат не принесет нужного эффекта. Антирезусный иммуноглобулин действует так:
- Разрушает в организме женщины эритроциты плода, которые успели попасть в ее кровь при родах или операции.
- Вследствие этого антитела не успевают образоваться.
- При следующей беременности риск резус-конфликта сводится к минимуму.

Симптомы
Если никаких сопутствующих заболеваний нет, то самочувствие женщины даже при резус-конфликте никак не меняется. Внешне обнаружить это отклонение нельзя. Для выявления патологии используются следующие исследования:
|
Метод диагностики |
Что показывает |
|
Анализ на резус-конфликт |
Увеличение содержания антител в крови. Опасными являются резкое повышение или скачкообразное изменение их титра. |
|
УЗИ |
|
|
Оценка уровня билирубина в околоплодной жидкости |
Оценивает интенсивность распада эритроцитов. |
Механизм возникновения

Если кровяные клетки резус-положительного плода попадают в кровеносное русло матери с Rh-, происходит активация иммунитета. Первичная выработка антител говорит о сенсибилизации организма. Смешивание крови матери и плода, как правило, происходит непосредственно во время родов, причем, риск такого развития событий увеличивается при кесаревом сечении либо при механическом отделении плаценты. При наступлении следующей беременности и вынашивании Rh+ плода срабатывает иммунная память. Иммунитет беременной начинает все более активно вырабатывать антитела в значительном количестве.
Читаем
-
Люди с постоянной болью часто думают, что эти страдания только от определенной болезни, будь то артрит, боли в спине, кишечнике, мигрень или что-то еще. Многие испытывают боль в течение нескольких месяцев или дольше.
-
Форма лечения глаукомы зависит от формы, стадии, сопутствующих заболеваний. Ключевой момент в лечении глаукомы является нормализация уровня внутриглазного давления.
-
Практически каждая беременная женщина наблюдает у себя симметричные коричневые пятна на лице вокруг щек, носа и лба, растяжки, варикозное расширение вен, изменение в росте волос, а также проходящий зуд кожи. Что же с этим делать?
-
При заболеваниях щитовидной железы аутоиммунного генеза ведущая роль в патологическом процессе принадлежит антителам, продуцируемым B-лимфоцитами человека к различным компонентам (антигенам) тиреоидной клетки.
-
Искривлённая перегородка и увеличенные носовые раковины являются одними из наиболее распространенных причин заложенности носа. При постоянно сохраняющихся симптомах рекомендуется оперативная помощь, цель которой — улучшение структуры носовых проходов.
Тактика ведения беременности в зависимости от полученных результатов обследования
- В срок беременности более 34 нед при наличии у пациентки дельта ОП-450 нм в зоне III или уровня фетального гематокрита ниже 30%, а также при ультразвуковых признаках водянки плода должно быть предпринято родоразрешение.
- В гестационный срок менее 34 нед при аналогичных показателях требуется либо внутриматочная гемотрансфузия, либо родоразрешение.
Окончательное решение должно быть принято на основании оценки зрелости легких плода, данных акушерского анамнеза и нарастания уровня билирубина в амниотической жидкости и возможностей перинатальной службы. Если нет условий для проведения внутриматочных гемотрансфузий, следует провести профилактику респираторного дистресс-синдрома кортикостероидами в течение 48 ч. Родоразрешение может быть предпринято спустя 48 ч после введения первой дозы кортикостероидов. Необходимо помнить, что после введения кортикостероидов снижаются показатели дельты 459 нм, при этом врач не должен считать это признаком улучшения течения заболевания.
Если срок гестации менее 34 нед, легкие плода незрелые и есть возможность для проведения внутриматочных гемотрансфузий, то приступают к их проведению.
Методы проведения внутриматочных гемотрансфузий
Существуют 2 метода проведения внутриматочных гемотрансфузий: внутрибрюшинная — введение эритроцитной массы непосредственно в брюшную полость плода (метод в настоящее время практически не используется); внутрисосудистая — введение эритроцитной массы в вену пуповины.
Внутрисосудистая гемотрансфузия является методом выбора в связи с меньшим риском осложнений и возможностью контроля за тяжестью анемии и эффективностью лечения. Кроме того, при внутрисосудистой гемотрансфузии возможен больший интервал между трансфузиями и роды могут быть отсрочены до достижения плодом более зрелого гестационного возраста.
Внутрисосудистая гемотрансфузия
Техника. Под контролем УЗИ определяют положение плода и место пункции вены пуповины. Иглой 20-го или 22-го калибра трансабдоминально под контролем УЗИ пунктируют пупочную вену недалеко от места отхождения ее от плаценты. С целью обездвиживания плода внутрисосудисто (через пупочную вену) или внутримышечно плоду вводят миорелаксанты.
Гемотрансфузию проводят с начальной скоростью 1–2 мл/мин, постепенно доводя скорость до 10 мл/мин. До и после гемотрансфу-зии эритроцитной массы определяют гематокрит плода. Конечный гематокрит определяет адекватность гемотрансфузии. Желательный конечный гематокрит (после трансфузии) — 45%. При тяжелой анемии плода с гематокритом ниже 30% трансфузии позволяют поддерживать гематокрит на уровне, близком к нормальному для данного гестацион-ного возраста (45–50%).
Требования к эритроцитной массе: группа крови 0, резус-отрицательная, тестированная и негативная на вирус гепатита В, С, цитомегаловирус и ВИЧ, совместимая с матерью и плодом, отмытая в физиологическом растворе для сведения к минимуму риска вирусного заражения.
Интервал между трансфузиями зависит от посттрансфузионного гематокрита и составляет в среднем 2–3 нед.
Внутрисосудистая гемотрансфузия обеспечивает:
- подавление продукции фетальных эритроцитов (в ответ на меньшее количество резус-положительных клеток снижается стимуляция материнской иммунной системы);
- пролонгировать беременность до более зрелого гестационного возраста плода и предотвратить осложнения, связанные с глубокой недоношенностью.
Осложнения:
- гибель плода (в отсутствие водянки плода в 0–2% случаев, при водянке плода в 10–15% случаев);
- брадикардия у плода в 8% случаев;
- амнионит в 0,5% случаев;
- кровотечение из места пункции в 1% случаев;
- преждевременный разрыв плодных оболочек в 0,5% случаев.Оценить осложнения непросто в связи с тем, что лечению подвергаются тяжело больные плоды.
Прогрессирование или регресс водянки плода может быть прослежен при УЗИ, позволяющем определить показания для повторной трансфузии. В 60–70% случаев через 2–3 нед требуется повторная трансфузия. Амниоцентез имеет малую ценность после проведения внутриматочной гемотрансфузии, когда околоплодные воды обычно загрязнены кровью. При этом возможно ложное повышение уровня билирубина в амниотической жидкости.
Роды должны быть предприняты только тогда, когда риск, связанный с преждевременными родами, меньше риска, связанного с внутриматочной трансфузией. В типичных случаях это происходит к 34-й неделе гестации. Кесарево сечение является оптимальным методом родоразрешения при водянке и тяжелой анемии у плода, когда имеется высокий риск нарушения его состояния в родах. Во время родов должна присутствовать неонатальная бригада, имеющая в своем распоряжении кровь для заменного переливания.
Описание
Резус-фактор (Rh) — это антиген (белок), который находится на поверхности эритроцитов, причём наиболее иммуногенным является антиген D (RhD), присутствие которого и определяет положительный резус-фактор (Rh+). Исследование выполняется с 9 полных недель беременности, т. е. с 10 недели.Для проведения исследования необходимо предоставить копию УЗИ.
Если резус-отрицательная (Rh-) женщина беременна резус-положительным (Rh+) плодом, её иммунная система начинает вырабатывать анти-D-антитела, вызывающие разрушение эритроцитов плода. Как правило, анти-D-антитела отсутствуют при первой беременности Rh+ плодом, протекающей без осложнений, однако сенсибилизация матери возникает в процессе родов. При каждой последующей беременности или при повреждении плаценты увеличивается риск развития гемолитической болезни плода. 98% случаев гемолитической болезни новорождённых связаны именно с D-резус-антигеном. При раннем проявлении резус-конфликт может стать причиной нарушения развития плода, преждевременных родов или выкидышей.Ген RHD
Делеция гена RHD в обеих гомологичных хромосомах обуславливает отрицательный резус-фактор. Наличие гена в гомозиготном или гетерозиготном состоянии определяет положительный резус-фактор у обследуемого. В случае если резус-положительные отцы являются гетерозиготными по резус-фактору, то у резус-отрицательных матерей даже при наличии отягощённого анамнеза плод в 50% случаев будет резус-отрицательным. Таким образом, для женщин с резус-конфликтной беременностью появилась возможность проведения пренатальной диагностики с целью определения резус-фактора на ДНК плода, выделенной из ворсин хориона (10–15 недель беременности) или из амниотической жидкости при проведении амниоцентеза (24 неделя беременности).
Если результаты молекулярно-генетического анализа показывают, что плод является резус-отрицательным, то отпадает необходимость в проведении последующих инвазивных процедур, и такие пациентки исключаются из дальнейшего обследования по тяжести развития гемолитической болезни плода. Кроме того, определение гетерозиготного генотипа по резус-фактору (RHD+/RHD-) у отца даёт основание для проведения преимплантационной диагностики при наличии отягощённого акушерского анамнеза (гибель детей от гемолитической болезни) и резус-сенсибилизации у матери. В результате при ЭКО будущей матери будут перенесены только резус-отрицательные эмбрионы.
Так как антирезусную профилактику иммуноглобулином человека рекомендовано проводить на 28 неделе первой и последующих беременностей, то определение резус-фактора плода на ранних сроках является необходимым. Определение Rh- плода в 1–2 триместре беременности позволит сократить расходы на регулярное определение титра анти-D-антител и антирезусную профилактику.Показания
Беременным (Rh-)-женщинам с 12 по 27 неделю беременности, если (Rh+)-отец является гетерозиготным носителем гена RhD (Генотипирование системы RhD).Подготовка
Специальная подготовка не требуется. Рекомендуется взятие крови не ранее чем через 4 часа после последнего приема пищи.Интерпретация результатов
При отрицательном результате теста, статус плода считается с высокой вероятностью резус-отрицательным, однако рекомендуется повторять тест на более поздних сроках беременности (но не позднее 27-ой недели) для подтверждения.
Положительный результат теста считается показанием к введению антирезусного иммуноглобулина, однако вопрос о его введении должен решаться только акушером-гинекологом на основании и других методов диагностики резус-конфликта.
При отсутствии антител к Rh-фактору по результатам ИФА и положительном молекулярно-генетическом тесте, рекомендуется введение антирезусного иммуноглобулина в период от 28 недель беременности (для профилактики ГБН) и не позднее 72 часов после родов (для профилактики Rh-конфликта при следующей беременности).
Закон Менделя
На основе открытия Карла Ландштайнера, выяснившего наличие антигенов крови, ныне существует закон Менделя о наследовании ее группы. Хотя Грегор Мендель жил в XIX веке и был монахом, его учение о передаче биологических признаков от родителей детям оказались не далеки от истины и сегодня они объяснены с точки зрения молекулярных механизмов наследования генов. И выглядит это так. Первая группа крови характеризуется отсутствием антигенов А и В. Это значит, что та группа крови, в которой данные антигены есть — (вторая, имеет только А, третья -только В, четвертая — А и В) никогда не сможет оказаться у ребенка, чьи родители имеют первую группу. Если у мужа и жены первая и вторая группа крови, тогда их дети будут наследниками отцовской или материнской группы, в зависимости от наличия у них доминантных или рецессивных фенотипических признаков. Аналогичная ситуация возникает в браке у людей с первой и третьей группой крови. Но вот
у родителей с четвертой группой могут быть дети, обладающие или второй, или третьей, или даже четвертой. Потому что во всех этих группах есть антигены А и В, в том или ином количестве, а значит, под воздействием все того же кодоминантно-рецессивного типа сформируется та или иная выше указанная группа. Но вот только не первая, потому что в ней антигенов А и В изначально нет. Если у родителей вторая и третья группы крови, тогда то, какая сформируется у ребенка, предсказать абсолютно невозможно. Малыш может стать обладателем любой группы крови из четырех, но опять же это связано исключительно с влиянием доминантных и рецессивных генов его родителей.
Ныне генетиками и гематологами уже зафиксированы исключения, получившие название «бомбейский феномен». У некоторых людей в генетическом материале было обнаружено присутствие А и В антигенов при том, что по анализами крови эти представители оказались обладателями первой группы. То есть данные антигены и все их признаки не проявляются фенотипически. Но пока эта редкость была зафиксирована только у нескольких индийцев и данный «бомбейский феномен» детально исследуется учеными многих стран мира.
Патологическая анатомия
Патологоанатомические изменения при внутриутробной смерти плода при сроке беременности V—VII мес. (ранняя фетопатия) скудные. Изучение их затрудняется из-за аутолиза и мацерации.
Рис. 21. Эритробластоз печени. Обилие эритробластов и нормобластов (темные клетки) в синусоидах печени при отечной форме гемолитической болезни новорожденных (окраска гематоксилин-эозином; х 400).
Рис. 22. Накопление гемосидерина (синего цвета) в макрофагах красной пульпы селезенки при желтушной форме гемолитической болезни новорожденных (окраска по Перльсу; х 400).
Рис. 23. Острое набухание, ишемические изменения нейронов (указано стрелками) в аммоновом роге головного мозга при желтушной форме гемолитической болезни новорожденных (окраска по Нисслю; х 400).
Отечная форма Г. б. н. характеризуется общими значительными отеками, кожа плода бледная, полупрозрачная, блестящая, частично мацерированная, с петехиальными кровоизлияниями. В полостях тела — транссудат, количество к-рого достигает 30% веса тела плода (800 мл). Сердце, печень и селезенка значительно увеличены. Почки плотны и полнокровны, сохраняют выраженную эмбриональную дольчатость. Мягкая мозговая оболочка и ткань мозга отечны и полнокровны. Вил очковая железа атрофична. Имеются признаки недоношенности: задержка формирования ядер окостенения и др. При микроскопическом исследовании определяется значительный эритробластоз в печени (цветн. рис. 21), селезенке, лимф, узлах, почках. В костном мозге — преобладание ядросодержащих клеток эритроцитарного ряда. Отмечается умеренный гемосидероз органов. В сердце находят гиперплазию мышечных волокон. В печени, надпочечниках, головном мозге отмечаются кровоизлияния, дистрофические и некробиотические изменения, плазматическое пропитывание и фибриноидные изменения мелких сосудов. Изменения головного мозга характерны для состояния хронической гипоксии. Даже у доношенных плодов имеются признаки тканевой незрелости. Плацента отечна, с признаками преждевременной инволюции.
При анемической форме Г. б. н. выражены общая бледность покровов и малокровие внутренних органов. В печени и селезенке находят умеренный эритробластоз. Дистрофические и некробиотические изменения в органах незначительные. Изменения головного мозга выражены менее резко, чем при отечной форме. Смерть может наступить в период новорожденности от интеркуррентного заболевания.
Жeлтушная форма Г. б. н. характеризуется желтушностью покровов. В желтый цвет прокра-щены также подкожный жировой слой и интима крупных сосудов. Количество непрямого билирубина в сыворотке крови может достигать 20—40 мг% . В брюшной и плевральной полостях, в полости перикарда— небольшое количество прозрачной жидкости желтого цвета. Ядра головного мозга — гиппокамп, область дна ромбовидной ямки, нижние оливы, ядро подбугорья, бледное ядро, зубчатое ядро мозжечка — интенсивно прокрашиваются билирубином в охряно-желтый цвет (так наз. ядерная желтуха). Печень и селезенка увеличены. Последняя плотная, коричнево-красная на разрезе. В почках развиваются билирубиновые инфаркты (см.). В миокарде выявляются дистрофия и вакуолизация мышечных волокон. При микроскопическом исследовании обнаруживают дистрофические и некротические изменения (острое набухание, ишемические изменения) ганглиозных клеток головного мозга (цветн. рис. 23). Тяжесть поражения мозга усугубляется гипоксией из-за повреждений мелких сосудов. В печени и селезенке резко выражен гемосидероз (цветн. рис. 22), но эритробластоз менее значительный, чем при отечной форме. В печени, кроме того, обнаруживают желчные стазы, тромбы, иногда с образованием желчных камней.
Патогенез
Патогенез: эритроциты плода содержат резус-фактор (Rh), унаследованный от «резус-положительного» отца, который может быть гомозиготом (Rh Rh) или гетерозиготом (Rh rh); мать — «резус-отрицательная» (rh), ее эритроциты не содержат резус-фактора, в связи с чем он по отношению к организму матери является антигеном. Через плаценту резус-фактор попадает от плода в кровь матери и вызывает у нее образование анти-Rh-агглютининов. Происходит изоиммунизация «резус-отрицательной матери» «резус-положительным плодом». Образовавшиеся анти-Rh-агглютинины поступают через плаценту от матери к плоду и вызывают у него гемолиз с последующим развитием анемии. В этом случае говорят о «резус-конфликте» между матерью и плодом. Во время родов, когда нарушается целость плацентарного барьера, в кровь рождающегося ребенка поступает особенно много анти-Rh-агглютининов, резко усиливается гемолиз его эритроцитов и нарастают клин, явления Г. б. н. Анти-Rh-агглютинины, получаемые ребенком с молоком матери, еще более усиливают у него гемолиз.
Нарушение билирубинового обмена, обусловленное интенсивным гемолизом, начинающимся еще в период внутриутробного развития, усугубляется несовершенством процессов конъюгации непрямого билирубина вследствие незрелости в печени фермента глюкуронилтрансферазы, в результате чего нарушается детоксикация непрямого билирубина и превращение его в нетоксичный прямой билирубин (диглюкуронидбилирубин).
AHTn-Rh-агглютинины образуются приблизительно у 3—5% женщин с резус-отрицательной кровью при беременности плодом с резус-положительной кровью. Повторные беременности «резус-отрицательной женщины» плодами с резус-положительной кровью, а также сделанные такой женщине раньше, иногда даже в детстве, повторные внутривенные или внутримышечные трансфузии резус-положительной крови способствуют более интенсивному образованию у нее анти-Rh-агглютининов при беременности «резус-положительным плодом». Имеют значение также состояние реактивности организма «резус-отрицательной матери», проявляющееся в повышении чувствительности к иммунизации резус-фактором, состояние эндокринной системы, имеющиеся хрон, или перенесенные в период беременности острые заболевания, повышающие проницаемость сосудистой стенки, особенно сосудов плаценты, частые искусственные прерывания беременности и т. д.
Имеет также значение и так наз. иммунологическая толерантность к резус-фактору: у «резус-отрицательных женщин», родившихся от «резус-положительных матерей», редко бывает изоиммунизация при беременности «резус-положительным плодом» (Р. А. Авдеева, 1965).
По-видимому, с этими факторами связано то, что Г. б. н. развивается не у каждого ребенка, рожденного от «резус-отрицательной матери» и «резус-положительного отца», а только у одного из 25—30.
Резус-фактор не является однородным, имеется несколько наиболее частых типов, обозначаемых Rh0, Rh0′, Rh0″, по А. Винеру, или cDe, CDe, cDE, CDE, по Фишеру— Рейсу. Резус-конфликт возникает чаще всего при несоответствии по Rh0(D), реже по другим, более слабым, антигенам. Г. б. н. возможна при несоответствии крови матери и плода по другим факторам: M, N, Hr, Kell, Kidd, Duffy. Несоответствие эритроцитов по основным группам крови AB0 также может вести к серол, конфликту: чаще всего конфликт наступает, когда ребенок (плод) имеет группу крови А или В, а мать группу 0 (см. Группы крови).