Когда кишечная палочка больше не несет пользу, или как бороться с симптомами эшерихиоза
Содержание:
Цистит – воспаление мочевого пузыря
Острый цистит у людей до 50 лет относится только к женщинам. Это воспаление слизистой, иногда более глубоких слоев стенки мочевого пузыря.
Цистит
Симптомы:
- внезапное начало;
- симптомы раздражения мочевого пузыря (поллакиурия, позывы, болезненное мочеиспускание);
- боль над лобковым сочленением;
- в моче обнаруживаются эритроциты, лейкоциты и многочисленные бактерии.
У молодых женщин с дизурией обычно развивается один из трех типов инфекции: воспаление мочевого пузыря, уретры или влагалища. Эти заболевания различают на основании клинических симптомов и результатов лабораторных исследований мочи.
|
Диагноз |
Пиурия |
Гематурия |
Бактериурия |
|
Цистит |
как правило |
иногда |
От 100 до 100 тысяч |
|
Уретрит |
как правило |
редко |
до 100 |
|
Вагинит |
редко |
редко |
до 100 |
При вагините наблюдаются выделения, зуд во влагалище, боль во время полового акта, но нет поллакиурии или болезненных позывов к мочеиспусканию.
Лечение цистита следует проводить от 3 до 7 дней. При неосложненной форме эффективность 3-дневного лечения такая же, как и при 7-дневном лечении, но было обнаружено меньше побочных эффектов.
Урологи используют более длительное лечение у женщин в случае следующих условий:
- беременность, сахарный диабет;
- симптомы продолжаются более 7 дней;
- вагинальная контрацепция;
- возраст старше 65 лет.
Бессимптомная бактериурия
Чаще всего обнаруживается случайно при плановых периодических осмотрах, так как отсутствуют субъективные симптомы, побуждающие пациента обращаться за медицинской помощью, и не обнаруживается заметных изменений со стороны мочевыделительной системы.
При отсутствии сопутствующих нарушений оттока мочи течение обычно легкое и не требует лечения. У пациентов с нарушением проходимости мочевыводящих путей симптомы обычно не проходят спонтанно. Этой группе пациентов рекомендуется антибактериальное лечение.
Дополнительно лечение следует начинать в следующих случаях:
- беременность (риск пиелонефрита, преждевременных родов, низкой массы тела новорожденного);
- перед плановой операцией (в основном на мочевыводящих путях);
- диабет.
В первом триместре беременности перед началом лечения ИМП всегда следует проводить антибиотикограмму.
Плазмиды
Кишечные палочки могут содержать различные плазмиды (см.): профаг, F (фактор фертильности), Col (колициногенный фактор), R (фактор резистентности), К88 (антигенный фактор), Ent (энтеротоксигенный фактор) и др. Профаги могут вызывать изменения отдельных признаков К. п., напр. О-антигена (см. Лизогения). F-плазмиды определяют половую полярность и вызывают образование половых ресничек (sex-pili). Col-плазмиды контролируют образование колицинов, подавляющих рост филогенетически родственных бактерий. R-плазмиды ответственны за резистентность К. п. к антибиотикам. Плазмида К88 контролирует синтез одноименного антигена и нитей, определяющих адгезивные свойства энтеропатогенных и энтеротоксигенных К. п.; плазмиды могут быть двух типов. Один из них определяет синтез термолабильного, другой — термолабильного и термостабильного энтеротоксина.
Экология
Резервуаром Кишечной палочки в природе является человек, толстая кишка к-рого заселяется разными биотипами этого микроба с момента перехода ребенка на смешанное питание, примерно к концу первого года жизни. Количество К. п. в 1 г испражнений колеблется от нескольких миллионов до 1—3 млрд. особей. На протяжении жизни человека происходит многократная смена биотипов К. п. в кишечнике. Определенную роль в этом процессе играет режим питания, перенесенные инфекции, лечение химиопрепаратами, антибиотиками и другие факторы. В естественных условиях К. п. обитает также в кишечнике домашних животных, птиц, диких млекопитающих, рептилий, рыб и многих беспозвоночных.
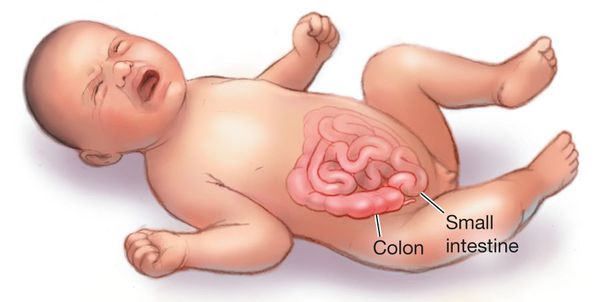
Причины кишечной инфекции у новорожденного
Заражение кишечной инфекцией происходит всегда орально-фекальным путем, т.е. бактерии из кишечника с испражнениями попадают на руки, затем на различные предметы. Как известно, дети с первых месяцев жизни пытаются затянуть в рот любой предмет, попавший им в руки, это является частью саморазвития, но в то же время, грозит тяжелыми последствиями.
В организм новорожденных бактерии проникают обычно из-за несоблюдения родителями простых гигиенических требований по уходу за ребенком, например, инфекция может возникнуть из-за плохо вымытой бутылочки, упавшей соски (особенно на улице), немытые руки и пр.
Кроме этого, заражение может произойти через организм матери, которая может быть носителем опасных бактерий или заразиться инфекцией во время беременности. Заражение ребенка может произойти еще в утробе матери (при заглатывании околоплодных вод, через общий кровоток с матерью) либо в момент рождения, при прохождении через родовые пути.
Уретрит
Чаще всего заболевание связано с половым контактом, катетеризацией или эндоскопией мочевого пузыря. Уретрит всегда возникает у пациентов с постоянно введенным мочевым катетером. Отверстие уретры красное, пациенты жалуются на ряд симптомов:
- жгучая боль и зуд в уретре;
- подтекание слизистого, стекловидного или гнойного отделяемого;
- боль внизу живота.
До недавнего времени наиболее частой причиной уретрита была гонорея. Теперь инфекция в два раза чаще вызываются Chlamydia trachomatis и Ureoplasma urealyticum. В 30% случаев инфекция гонореи сосуществует с двумя другими.
Уретрит
Стандартный посев мочи часто бывает стерильным, после чего проводят иммунологические тесты и выделяют микроорганизмы на специально подготовленных средах.
Наиболее распространенные методы лечения – однократный прием фторхинолонов и доксициклина в течение 7 дней.
Классификация
Вагинит бактериальный классифицируется гинекологами в зависимости от происхождения, формы, локализации очага и причин, вызвавших воспаление.
По происхождению:
- неспецифический – возникает в виде дисбактериоза при нарушении баланса нормальной влагалищной флоры
- специфический – инфицирование вирусами и бактериями, не характерными для физиологического состава
По форме:
- острый – протекает с ярко выраженной симптоматикой, может переходить в ткани шейки матки и вульвы
- хронический – характерно «вялое» течение, иногда симптоматика мало заметна или отсутствует, периодически возникают обострения
- подострый – симптомы острого вагинита постепенно проходят, но патологический процесс в слизистой продолжается
- рецидивирующий – разновидность хронической формы, развивается при неправильном лечении, либо при повторном инфицировании половым путем на фоне проведенной терапии
По локализации очага:
- первичный – процесс возникает и развивается непосредственно во влагалище
- вторичный – воспаление переходит из органов, расположенных рядом (нисходящий – из матки или шейки, восходящий – из наружных органов)
Первичный бактериальный вагинит у женщин репродуктивного возраста встречается чаще, чем вторичный.
В зависимости от причины:
- Кандидозный – вызван активно размножающимися организмами грибкового происхождения. Кандидоз развивается при инфицировании во время сексуального контакта, либо в результате иммунного сбоя в организме женщины.
- Атрофический – неспецифический бактериальный вагинит. Имеет гормональную природу. Формируется на фоне недостатка эстрогенов.
- Хламидийный – провоцируется хламидиями и поражает все отделы половой системы – маточные трубы, матку, влагалище.
- Гонорейный – протекает остро при попадании возбудителя в половые пути.
- Трихомонадный – поражение органов трихомонадами в быту через предметы личной гигиены, либо половым путем.
- Мико- или уреаплазменный – часто обнаруживается случайно при обследовании. Клинически не проявляется.
Бактериальный вагинит (кольпит) бывает вызван несколькими причинами. Выяснить этиологию заболевания возможно при инструментальном осмотре и по лабораторным показателям.
- Врачи клиники АВС не просто проводят лечение, но и единственная в России клиника со своей авторской программой.
- Решение проблем, связанных с интимной жизнью.
- Эффективные меры при хронической форме заболевания.
- Мы лечим заболевание, а не симптомы.
Лечение
Для лечения симптомов кишечной палочки у взрослых и детей используются такие группы препаратов:
- Антибактериальные средства. Традиционное лечение кишечной палочки в моче, во влагалище у женщин и в просвете толстого кишечника, включает прием антибиотиков из группы цефалоспоринов. Курс лечения составляет от 5 до 10 дней.
- Спазмолитики и обезболивающие препараты. Обезболивающие таблетки для лечения симптомов кишечной палочки у взрослых и детей назначаются при выраженном болевом синдроме. С лечебной целью назначаются такие препараты, как Нурофен, Спазмалин, Но-шпа.
- Пробиотики. Эта группа лекарственных средств помогает восстановить баланс нормальной микрофлоры в просвете толстого кишечника и во влагалище у женщин.
Для того чтобы пробиотики, содержащие бифидум и лактобактерии, могли эффективно восстановить микрофлору, их приём необходимо сочетать с пребиотиками, которые создают благоприятную среду для размножения полезных бактерий. Высокую результативность при эшерихиозе доказал комбинированный препарат Стимбифид Плюс, который относится к метапребиотикам, и содержит уникальную комбинацию фруктополисахаридов и фруктоолигосахаридов.
Метапребиотик Стимбифид Плюс обеспечивает микрофлору толстого кишечника и влагалища уникальным питанием, чем стимулируют её размножение. На основании полученных результатов клинических исследований, была составлена сравнительная характеристика эффективности Стимбифид Плюс и других препаратов, влияющих на состав кишечной микрофлоры. Метапребиотик доказал свое абсолютное лидерство. Биодобавка Стимбифид Плюс одинаково эффективна для профилактики как эшерихиозов, так и для их других заболеваний.
Терапия дисбактериоза
Лечебные мероприятия по восстановлению состава микрофлоры могут потребовать продолжительного времени. Для того чтобы терапия была эффективной , необходимо обратиться к специалисту, который после ряда обследований и на основании жалоб больного сможет подобрать максимально эффективное средство от дисбактериоза.
При любом течении заболевания лечение включает в себя следующие пункты:
-
прием лекарственных препаратов, помогающих нормализовать микрофлору кишечника и восстановить баланс между полезными и патогенными микроорганизмами;
-
включение в терапию бактериофагов, которые помогают подавить рост и численность вредных бактерий, предназначенных для лечения 1 и 2 степени дисбиоза;
-
соблюдение правил питания, которое заключается в исключении группы продуктов, способствующих размножению вредных бактерий и включениепробиотических продуктов, богатых живыми полезными микроорганизмами
От того, насколько будет правильно и эффективно проведено лечение зависит дальнейшее состояние здоровье кишечника
Поскольку флора кишечника очень чувствительна к внешним раздражителям, то очень важно соблюдать все рекомендации по комплексному лечению и методам профилактики, что поможет снизить до минимума риск развития дисбиоза в будущем
Терапия дисбиоза основывается не только на тяжести течения болезни, но и причинах развития. Эффективность и исход лечения может быть только при условии комплексного подхода, который состоит из следующих восстановительных мероприятий:
-
восстановление уровня бактерий;
-
восстановление опорожнения кишечника;
-
восстановление иммунной защиты;
-
возобновление транспортировки питательных веществ, получаемых из пищи в межклеточное пространство, кровь и лимфатическую систему.
Лекарственные препараты позволяютвосстановить микрофлору кишечника, устранить неприятную симптоматику болезни, а также скорректировать иммунитет.
Наиболее эффективно восстанавливает бифидумбактерии и лактобактерии в кишечнике кисломолочный пробиотический продукт лечебно-профилактического питания бифилакт БИОТА, в котором эти бактерии находятся в живом состоянии, что позволяет им адгезироваться (прикрепляться) не стенки кишечника и эффективно размножаться ( БИФИЛАКТ БИОТА ДЛЯ ЛЕЧЕНИЯ ДИСБАКТЕРИОЗА У ВЗРОСЛЫХ)
Симптомы
Симптомы болезней, вызываемых бактериями STEC, включают абдоминальные спазмы и диарею, которая в некоторых случаях может переходить в кровавую диарею (геморрагический колит). Возможны также лихорадка и рвота. Инкубационный период длится от 3 до 8 дней, при средней продолжительности 3-4 дня. Большинство пациентов выздоравливает в течение 10 дней, но у незначительного числа пациентов (особенно детей раннего возраста и пожилых людей) инфекция может приводить к развитию такой представляющей угрозу для жизни болезни, как гемолитический уремический синдром (ГУС). Для ГУС характерны острая почечная недостаточность, гемолитическая анемия и тромбоцитопения (низкий уровень тромбоцитов в крови).
Люди, страдающие от кровавой диареи или тяжелых абдоминальных спазмов, должны обращаться за медицинской помощью. Антибиотики не являются составной частью лечения пациентов с болезнью, вызванной STEC, и могут повышать риск развития ГУС.
По оценкам, ГУС может развиваться у 10 % пациентов с инфекцией STEC, а коэффициент летальности составляет от 3 до 5 %. Во всем мире ГУС является самой распространенной причиной острой почечной недостаточности у детей раннего возраста. Он может приводить к неврологическим осложнениям (таким как конвульсии, инсульт и кома) у 25 % пациентов и к хроническим заболеваниям почек, обычно нетяжелым, примерно у 50 % выживших пациентов.
Резистентность
Устойчивость Кишечной палочки к воздействию внешних факторов — обычная для аспорогенных бактерий. Во внешней среде (воде, почве) она выживает в зависимости от конкретных условий в течение нескольких месяцев При нагревании во взвесях погибает при 55° через час, при 60° — через 15 мин., в 1% р-ре фенола — через 10 мин., в р-ре сулемы 1:4000 — через 2 мин. К. п. обладает избирательной чувствительностью к бриллиантовому зеленому и солям тетратионовой к-ты. На этом основано применение ряда селективных сред. Многие штаммы К. п. высокочувствительны к мономицину, канамицину, гентамицину.
Методы выделения и идентификации. Материалом для выделения К. п. являются объекты внешней среды (вода, почва, смывы с разных предметов), при заболеваниях — испражнения, рвотные массы, моча, дуоденальное содержимое или кровь, а также пищевые продукты, подозреваемые как источник заражения. Материал засевают на дифференциально-диагностические среды (см.) с последующим выделением чистой культуры К. п. Идентификацию последней проводят путем изучения морфологических, культуральных, биохимических и антигенных признаков. Заключительным этапом является определение биотипа Кишечной палочки, особенно серогруппы и серотипа.
См. также Escherichia.
Библиография: Борисов Л. Б. Энтеропатогенные кишечные палочки и их фаги, Л., 1976, библиогр.; Кауфман Ф. Семейство кишечных бактерий, пер. с англ., М., 1959, библиогр.; Методы санитарно-микробиологического исследования объектов окружающей среды, под ред. Г. И. Сидоренко, М., 1978; Минкевич И. Е. Бактерии группы кишечной палочки как санитарно-показательные микроорганизмы, Л., 1949; Острые кишечные инфекции, под ред. Т. В. Перадзе, с. 73, Л., 1973, библиогр.; Tабачник А. Л., Гиршович Е. С. и Темпер Р. М. Энтеротоксигенные Е. coli, Журн, микр., эпид, и иммун., № 3, с. 31, 1977, библиогр.; Bergey’s manual of determinative bacteriology, ed. by R. E. Buchanan a. N. E. Gibbons, Baltimore, 1975, bibliogr.; Cooke E. M. Escherichia coli and man, Edinburgh—L., 1974; Medearis D. N., Cammitta B. M. a. Heath E. C. Cell wall composition and virulence in Escherichia coli, J. exp. Med., v. 128, p. 399, 1968; Orskov I. a. o. Serology, chemistry and genetics of O and К antigens of Escherichia coli, Bact. Rev., v. 41, p. 667, 1977, bibliogr.
Источники
- Schaeffer A.: Инфекции мочевыводящих путей. Урология Кэмпбелла, 1992.
- Набер К.Г. и др.: Рекомендации по лечению инфекций мочевыводящих путей и мужских половых путей, 2000.
- Гриневич В. и др.: Инфекции мочевыводящих путей. Урологический обзор, 2000.
- Safir MH et al.: Инфекции мочевыводящих путей: просто и сложно, 1998.
- Эйчман В.: Лечение бактериальных инфекций органов мочеполовой системы. Урологическое обозрение, 2000.
- Macfarlane MT: Инфекции мочевыводящих путей, 1997.
ОНЛАЙН-ЗАПИСЬ в клинику ДИАНА
Вы можете записаться по бесплатному номеру телефона 8-800-707-15-60 или заполнить контактную форму. В этом случае мы свяжемся с вами сами.
Чума плотоядных
Относится к одним из самых опасных заболеваний у плотоядных животных. Даже при грамотном и своевременном лечении инфекция может привести к летальному исходу, при этом клиническая картина отличается разнообразием.
Путь заражения и длительность заболевания
Распространение инфекции осуществляется оральным или воздушным путем, через миску животного, остатки его еды, через выделения. Иногда наблюдается внутриутробный путь инфицирования, когда у собаки отсутствует иммунный ответ. В этом случае чаще поражается центральная нервная система (25%-75% собак имеет характерные признаки).
Инкубационный период этой болезни — от 2-х дней до 2-3 недель. Длительность острого периода течения заболевания 2-4 недели. Иногда оно переходит в хроническую форму, длительностью до нескольких месяцев.
Летальность от чумы плотоядной – 80%-90% среди щенят.
Симптомы чумы плотоядных
- Сонливость, апатичность, вялость.
- Собака пытается укрыться в темном месте.
- Отсутствие аппетита.
- Температура до 40-41 градуса.
- Гнойные выделения из глаз, язвенные поражения слизистой.
- Слизисто-гнойные выделения из глаз.
- Нарушение дыхательной функции, хрипы в легких.
- Рвота, диарея, иногда с примесью крови.
- Наличие мелкоточечной красной сыпи (не всегда).
- Гиперкератоз подушек лап (ороговение) – наблюдается на последней стадии, считается злокачественным поражением.
- Признаки негнойного менингоэнцефаломиелита (наблюдаются симптомы эпилепсии, припадка, и другие признаки поражения нервной системы), а также наблюдается паралич конечностей, что указывает на вовлечение в процесс спинного мозга. В этом случае уже основная часть нервных клеток поражена.
Лечение во всех случаях симптоматическое, так как целенаправленной терапии против чумы до сегодняшнего дня не разработано. Самый лучший способ борьбы с вирусом чумы – это своевременная вакцинация собак.
Какая диета при запорах у детей?
В этой статье мы постараемся раскрыть вопросы, наиболее часто задаваемые взрослыми, столкнувшимися с детскими запорами. Как организовать режим питания малыша, какая диета при запорах у детей? Прежде чем определиться с рационом, стоит понять, какие причины могут привести к закреплению стула у ребенка.
- Это может быть наследственная патология, откорректировать питанием, которую проблематично.
- Смена климатических зон (поездка на отдых): меняется характер климата, вода и питание.
- Определенное стечение факторов, приведших к обезвоживанию детского организма: рвота, малое потребление жидкости, большие объемы срыгивания.
- Низкая двигательная активность ребенка.
- Повреждение слизистой ануса. Из – за болевой симптоматики у малыша появляется боязнь дефекации.
- Ввод прикорма для грудничков.
- В случае если родители пытаются очень быстро приучить малышей ходить на горшок.
- Несбалансированное питание. Это, зачастую, главная проблема и причина детских запоров.
Постоянные конфеты, чипсы, сухарики, печенье. Вся эта еда всухомятку приводит не только к запорам, но и к дальнейшим осложнениям, способным развиться в более тяжелые патологии желудочно-кишечного тракта. Даже сам по себе шоколад, входящий в состав многих конфет, относится к скрепляющим продуктам. В такой ситуации только придерживание полноценного и сбалансированного рациона способно сдвинуть ситуацию к лучшему.
Так какая диета при запорах у детей? Ведь применять для малышей слабительные препараты не рекомендуется.
Правила детской диеты при запоре сродни взрослому диетическому рациону, но имеет свои и особенности. Прежде чем посадить малыша на диету, стоит пройти обследование, чтобы быть уверенным, что у ребенка нет более серьезных патологических изменений. Для этого стоит обратиться к своему участковому педиатру. Он, проанализировав результаты исследования, сможет указать причину запоров у ребенка, и если это последствия неправильного питания, вот тогда и следует заняться корректированием детского рациона. В противном случае, возможно малышу необходимо более серьезное лечение. Но даже в этой ситуации правильное питание не следует снимать с повестки дня.
Так что же такое диета – это исключение из рациона, или уменьшение количественной составляющей, продуктов питания, которые замедляют перистальтику кишечника, обладая обволакивающими характеристиками. Например, к таковым можно причислить такие блюда: рисовую кашу, тяжелые наваристые бульоны, шоколад, кашу их манки, кисели.
В рационе малыша должно присутствовать много фруктов и овощей. Они богаты витаминами и микроэлементами, так необходимыми для растущего организма. Полезны для желудка малыша и его перистальтики кисломолочные продукты.
Факторы патогенности кишечной палочки
Способность Е. coli вызывать различные заболевания обусловлена наличием у нее следующих факторов патогенности:
Факторы адгезии и колонизации. Они необходимы для прикрепления к клет кам ткани и их колонизации. Обнаружено три варианта фактора колонизации: а) CFA/I-CFA/VI (англ. colonization factor) — они имеют фимбриальную структуру; б) EAF (англ. enteropathogenic Е. coli adherence factor) — интимин — белок наружной мембраны, кодируется геном еаеА. Обнаружен у 4 и ЕНЕС, выявляется по спо собности бактерий прикрепляться к клеткам Нер-2; в) Adhesion Henle-407 — фимбриальные структуры, выявляются по способности бактерий прикрепляться к клет кам Henle-407. Все они кодируются плазмидными генами. Помимо них описаны и другие факторы колонизации, в роли которых могут выступать также бактериаль ные липополисахариды.
Факторы инвазии. С их помощью EIEC и ЕНЕС, например, проникают в эпителиоциты кишечника, размножаются в них и вызывают их разрушение. Роль факторов инвазии выполняют белки наружной мембраны.
Экзотоксины. У патогенных Е. coli обнаружены экзотоксины, повреждающие мембраны (гемолизин), угнетающие синтез белка (токсин Шига), активизирующие вторичные мессенджеры (англ. messenger — связной) — токсины CNF, ST, CT, CLTD, EAST.
Гемолизины продуцируют разные патогены, в том числе Е. coli. Гемолизин — порообразующий токсин. Он вначале связывается с мембраной клетки-мишени, а затем формирует в ней пору, через которую происходит вход и выход небольших молекул и ионов, что ведет к гибели клеток и лизису эритроцитов.
Токсин Шига (STX) был обнаружен вначале у Shigella dysenteriae, а затем сходный токсин (шигаподобный токсин) был обнаружен у ЕНЕС. Токсин (N-гликозидаза) блокирует синтез белка, взаимодействуя с 28S рРНК, в результате чего клетка гибнет (цитотоксин). Различают два типа шигаподобного токсина: STX-1 и STX-2. STX-1 по антигенным свойствам почти идентичен токсину Шига, a STX-2 отличается от токсина Шига по антигенным свойствам и, в отличие от STX-1, не нейтрализуется антисывороткой к нему. Синтез цитотоксинов STX-1 и STX-2 контролируется у Е. coli генами умеренных конвертирующих профагов 9331 (STX-1) и 933W (STX-2).
- Токсин L (термолабильный токсин) — АДФ-рибозилтрансфераза; связываясь с G-белком, вызывает диарею.
- Токсин ST (термостабильный токсин), взаимодействуя с рецептором гуанилатциклазы, стимулирует ее активность и вызывает диарею.
- CNF (цитотоксический некротический фактор) — белок деамидаза, повреждает так называемые RhoG-белки. Этот токсин обнаружен у UPEC, вызывающих инфекции мочевыводящих путей.
- CLTD-токсин — цитолетальный разрыхляющий токсин. Механизм действия изучен слабо.
- Токсин EAST — термостабильный токсин энтероагрегативных Е. coli (EAEC), вероятно, подобен термостабильному токсину (ST).
Эндотоксины-липополисахариды. Они определяют антигенную специфич ность бактерий (которая детерминируется повторяющейся боковой цепочкой Сахаров) и форму колоний (утрата боковых цепочек приводит к превращению S-колоний в R-колонии).
Таким образом, факторы патогенности Е. coli контролируются не только хромосомными генами клетки-хозяина, но и генами, привносимыми плазмидами или умеренными конвертирующими фагами. Все это свидетельствует о возможности возникновения патогенных вариантов Е. coli в результате распространения среди них плазмид и умеренных фагов. Ниже дана краткая характеристика 4 категорий Е. coli, вызывающих ОКЗ; сведений о недавно выделенных категориях DAEC и ЕАЕС в доступных нам источниках не найдено.
ЕТЕС включает 17 серогрупп. Факторы адгезии и колонизации фимбриальной структуры типа CFA и энтеротоксины (LT или ST, или оба) кодируются одной и той же плазмидой (плазмидами). Колонизируют ворсинки без их повреждения. Энтеротоксины вызывают нарушение водно-солевого обмена. Локализация процесса — область тонкой кишки. Заражающая доза 108-1010 клеток. Заболевание протекает по типу холероподобной диареи. Тип эпидемий — водный, реже пищевой. Болеют дети в возрасте от 1 года до 3 лет и взрослые.
Как предотвратить эшерихиоз?
Эшерихиоз можно предотвратить, если правильно обезвреживать кал инфицированных людей, соблюдать гигиену и тщательно мыть руки с мылом. Меры профилактики, которые могут оказаться эффективными в условиях детского сада, включают разделение инфицированных и неинфицированных детей по разным группам или разрешение инфицированным детям посещать данные учреждения после 2 отрицательных культуральных исследований кала. Пастеризация молока и тщательное приготовление говядины являются эффективными в профилактике пищевой передачи инфекции
Важно сообщать о случаях кровавой диареи органам здравоохранения, так как своевременное вмешательство последних может предотвратить возникновение новых случаев инфекции
Источники и передача инфекции
Имеющаяся о STEC информация относится, в основном, к серотипу O157:H7, так как с биохимической точки зрения его можно легко дифференцировать от других штаммов E. coli. Резервуаром этого патогенного микроорганизма является, в основном, крупный рогатый скот. Кроме того, значительными резервуарами считаются другие жвачные животные (такие как овцы, козы и олени), обнаруживаются и другие инфицированные млекопитающие (такие как свиньи, лошади, кролики, собаки, кошки) и птицы (такие как куры и индейки).
E. coli O157:H7 передается человеку, главным образом, в результате потребления в пищу зараженных пищевых продуктов, таких как сырые или не прошедшие достаточную тепловую обработку продукты из мясного фарша и сырое молоко. Загрязнение фекалиями воды и других пищевых продуктов, а также перекрестное загрязнение во время приготовления пищи (через продукты из говядины и другого мяса, загрязненные рабочие поверхности и кухонные принадлежности) также могут приводить к инфицированию. Примеры пищевых продуктов, явившихся причиной вспышек E. coli O157:H7, включают не прошедшие надлежащую тепловую обработку гамбургеры, копченую салями, непастеризованный свежевыжатый яблочный сок, йогурт и сыр, приготовленный из сырого молока.
Все большее число вспышек болезни связано с потреблением в пищу фруктов и овощей (включая ростки, шпинат, латук, капусту и салат), заражение которых может происходить в результате контакта с фекалиями домашних или диких животных на какой-либо стадии их выращивания или обработки. Бактерии STEC обнаруживаются также в водоемах, (таких как пруды и реки), колодцах и поилках для скота. Они могут оставаться жизнеспособными в течение нескольких месяцев в навозе и осадочных отложениях на дне поилок. Так же была зарегистрирована передача инфекции как через зараженную питьевую воду, так и через воды для рекреационного использования.
Близкие контакты людей являются одним из основных путей передачи инфекции (орально-фекальный путь заражения). Были зарегистрированы бессимптомные носители, то есть лица, у которых не проявляются клинические симптомы болезни, но которые способны инфицировать других людей. Период выделения бактерий STEC у взрослых людей длится примерно одну неделю или менее, а у детей этот период может быть более длительным. В числе значительных факторов риска инфицирования STEC отмечается также посещение ферм и других мест содержания сельскохозяйственных животных, где возможен прямой контакт с ними.
Лечение бактериального вагинита у женщин
Лечение бактериального вагинита зависит от причины, вызвавшей заболевание. После получения результатов лабораторного исследования врач подберет противомикробную терапию с учетом вида возбудителя. Назначаются препараты системного действия и лекарственные формы для местного применения (растворы, свечи, кремы, вагинальные таблетки). Антибактериальное лечение назначается курсом на 7-14 дней.
После лечения антибиотиками показано использование препаратов, восстанавливающих бактериальный баланс. С этой целью назначаются лекарства, содержащие лакто- и бифидобактерии и препараты, обеспечивающие среду для их размножения – пребиотики и пробиотики. Восстановление микрофлоры после бактериального вагинита – это длительный процесс, требующий не только лекарственной терапии, но и соблюдения диеты.
При атрофическом вагините необходима коррекция гормонального фона организма. Атрофический тип чаще формируется у женщин в период климакса. Это связано с резким снижением в крови эстрогенов. Назначаются гормональные препараты в качестве заместительного лечения – это замедляет процессы дегенерации слизистой оболочки.
Эпидемиология
Е. coli является представителем нормальной микрофлоры кишечного тракта всех млекопитающих, птиц, рептилий и рыб. Поэтому для выяснения вопроса, какие варианты Е. coli и почему вызывают эшерихиозы, потребовалось изучить антигенное строение, разработать серологическую классификацию, необходимую для идентификации патогенных серовариантов, и выяснить, какими факторами патогенности они обладают, т. е. почему они способны вызывать различные формы эшерихиозов.
У Е. coli обнаружен 171 вариант О-антигенов (01-0171), 57 вариантов Н-антигенов (H1-H57) и 90 вариантов поверхностных (капсульных) К-антигенов. Однако в действительности существует 164 группы по О-антигену и 55 серовариантов по Н-антигену, так как некоторые из прежних 0:Н-серогрупп были исключены из вида E. coli, но порядковые номера О- и Н-антигенов сохранились неизменными. Антигенная характеристика диареегенных Е.соli включает в себя номера О- и Н-антигенов, например, 055:116; 0157:Н7; О-антиген означает принадлежность к определенной серогруппе, а Н-антиген — ее серовариант. Кроме того, при более углубленном изучении О- и Н-антигенов выявлены так называемые факторные О- и Н-антигены, т. е. их антигенные субварианты, например: Н2а, Н2Ь, Н2с или 020, О20а, O20ab и т. п. Всего в список диареегенных Е. coli включено 43 О-серогруппы и 57 ОН-серовариантов. Список этот пополняется все новыми серовариантами.
Классификация инфекций мочевыводящих путей
В зависимости от локализации инфекции, возраста пациента, выраженности симптомов и наличия дополнительных заболеваний была предложена следующая классификация ИМП:
В зависимости от выраженности клинических симптомов:
- Симптоматические инфекции мочевыводящих путей.
а. простые – у людей без отягчающих факторов:
- острое воспаление нижних мочевыводящих путей;
- рецидивирующее воспаление нижних мочевыводящих путей;
- острый пиелонефрит.
Острый пиелонефрит
б. комплексные – у людей с отягчающими обстоятельствами:
- острое воспаление нижних мочевыводящих путей;
- рецидивирующее воспаление нижних мочевыводящих путей;
- острый пиелонефрит.
- Бессимптомная бактериурия:
а. у пациентов без дополнительных факторов риска;
б. у пациентов с дополнительными факторами риска.
В зависимости от локализации инфекции:
- Инфекции верхних мочевыводящих путей: почек, пузырно-тазовой системы, околопочечной области.
- Инфекция нижних мочевыводящих путей: мочевого пузыря, уретры.
Как лечатся мочевыводящие инфекции у новорожденных
У новорожденных детей антибиотик вводится парентерально, у большинства остальных детей орально. В случае чувствительности к препарату моча становится стерильной через 24 часа после начала лечения. При сохранении бактерий в моче во время лечения говорит о резистентности возбудителя к препарату. Другие симптомы воспаления сохраняются дольше, повышение температуры до 2-3 дней, лейкоцитурия до 3-4 дней, повышение СОЭ может наблюдаться до 3 недель. Длительность лечения антибиотиками в среднем составляет 10 дней.
У детей с циститом задачей лечения является освобождение от дизурии, которая у большинства проходит в течение 1-2 дней, поэтому прием антибиотика в течение 3-5 дней оказывается обычно достаточным. У детей с пиелонефритом необходимо предупредить персистенцию инфекции и сморщивание почки. У пациентов с высоким риском прогрессирования профилактика должна проводиться в течение нескольких лет. При проведении лечения необходимо проводить с родителями разъяснительную работу о необходимости профилактических курсов лечения, на возможный неблагоприятный прогноз при наличии факторов прогрессирования.
1. И.Е.Тареева. Нефрология. Руководство для врачей Медицина 2000 г.
2. Т.В. Сергеева, О.В. Комарова. Инфекция мочевыводящих путей. Вопросы современной педиатрии 2002 г.
Автор статьи врач-педиатр Гончарова М.В.
Источник Сибирский медицинский портал